Hjelp, burde jeg sende placenta til patologen? – og hva skal jeg bruke svaret til?
Publisert 15. desember 2025
Annetine Staff
Forskningsleder, Kvinneklinikken, Oslo universitetssykehus, og professor, Det medisinske fakultet, Universitetet i Oslo
Gitta Turowski
Overlege, Leder for Perinatal Patologi, Avdeling for Patologi, Oslo universitetssykehus
Hva skjer med Placentakapittelet i Veilederen for fødselshjelp?
Forrige utgave av Placentakapittelet ble ferdigstilt i 2020, med 6 forfattere.1 I 2025-26 revideres dette kapittelet, ved de sammen forfattere, komplettert med en medforfatter med fostermedisinsk ekspertise (Cathrine Ebbing, UiB/Haukeland). Dermed suppleres kapittelet med ultralydfunn gynekologen vil kunne vurdere for eksempel ved spørsmål om tvilling-til tvillingstransfusjoner. I tillegg har vi valgt å flytte «Abruptio»-delen av kapittelet til et foreløpig eget, nytt kapittel. Dette fordi temaet ikke omtales i noe annet kapittel i Veilederen, og denne kliniske problemstillingen er viktig for vaktgående leger. Flere tilbakemeldinger tyder på at abruptio-aspektet drukner i det omfattende placentakapittelet.
Det reviderte kapittelet (altså de to kapitlene, Placenta og Abruptio placenta) sendes på høring, i februar-mars 2026, til alle medlemmer av Norsk Gynekologisk Forening. Deretter diskuteres revisjonsforslagene på årets Veiledermøte på Losby Gods 23-24 april 2026. Dette gir deg som leser av Gynekologen en gyllen mulighet for å bidra til et enda bedre Placentakapittel.
Dagens praksis ved din avdeling? Ved ukompliserte vaginale fødsler registreres antakelig placentas vekt, navlesnor og hinner i elektronisk pasientjournal av jordmor. Men ved en komplisert fødsel der lege også er involvert, hva er praksis da ved din avdeling? Kanskje burde lege og jordmor samsnakkes om funn ved placentainspeksjon, slik at rekvisisjon til patolog blir best mulig? Det er faglig uheldig dersom det er divergerende beskrivelse av placenta-relaterte funn i et legenotat og et jordmornotat. Kanskje du skal sjekke hva din avdelings rutiner og bidra til å etablere enda bedre rutiner?
Hvilke forslag og anbefalinger gir Veilederen i fødselshjelp om undersøkelse av placenta, og hvorfor?
A) Makroskopisk undersøkelse --> Alle
Veilederen sier: «Vi anbefaler at placenta undersøkes og beskrives makroskopisk av jordmor eller gynekolog etter alle fødsler.»
Tre kliniske eksempler på at makroskopisk undersøkelse kan være nyttig for legen og pasient:
- Kvinnen sivblør vaginalt etter at placenta er ute. Nyttig for kliniker på vakt å vite om placenta og hinner ser komplette ut, eller om det er grunn til å mistenke fastsittende rester som hindrer uteruskontraksjon? Ikke minst er det fint for pasienten, som kanskje unngår langvarige blødningsproblemer, rester og infeksjon i en allerede slitsom barseltid.
- Placenta syntes å være helt løs og kom samtidig med fødselen av barnet. Barnet er overraskende slapt og virker tilveksthemmet. Var det noen tegn på eldre koagler på placentas maternelle flate? Var det noen impresjoner i placentas maternelle flate som tegn på at det har vært et eldre (organisert) koagel her? Abruptio, spesielt akutt, er veldig vanskelig å diagnostisere fra patologens side, og klinikernes (vakthavende lege) målrettede undersøkelse av slike tegn er derfor svært nyttige.
- Det er kommet en klagesak på fødselsutfallet til et barn som er forløst ved din avdeling, som viser seg å ha læringsvansker. Mor lurte på om morkaken ikke så normal ut ved fødselen, og om morkakehinnene var grønne. Hun har lest seg opp på temaet og spør om ikke morkakesvikt med et stresset foster kan ha gitt en lett surstoffmangel og dermed bidratt til læringsvanskene. Du finner kun summarisk beskrivelse av upåfallende vaginalfødsel, inntil vakuumforløsning på grunn av et protrahert forløp. CTG var ikke beskrevet som patologisk. Du finner ingen beskrivelse av placenta i journal eller journalnotat. Hadde du hatt en beskrivelse av normale hinner og placenta, hadde du kunnet berolige mor om at intet patologisk var observert ved fødselen.
B) Patologisk undersøkelse --> Noen, men absolutt ikke alle
Veilederen sier: «Vi foreslår at placenta sendes til patologisk anatomisk undersøkelse ved alle fødsler der det har vært maternelle og/eller føtale komplikasjoner i svangerskap og/eller fødsel, samt ved placentære komplikasjoner (slik som velamentøst navlesnorsfeste, retroplacentære hematom etc.)»
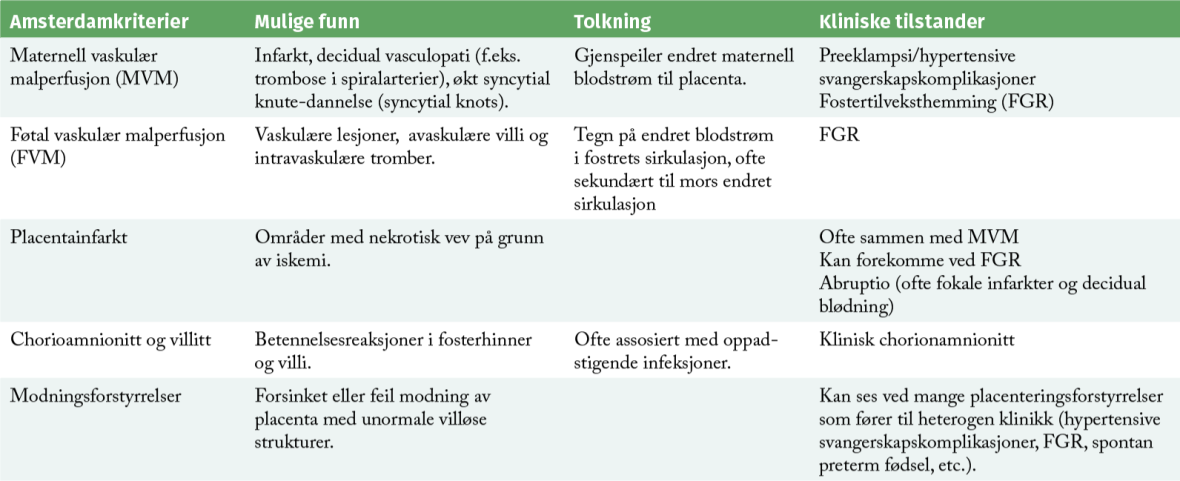
Historisk sett har det vært ulik praksis ved gjennomføring av patologenes undersøkelser av placenta (morfologiske analyser og immunhistokjemi). Undersøkelsesmetodikk og rapportering har i stor grad vært avhengig av patologens ekspertise og interesse for placenta. For å harmonisere rapportering av placentamorfologi har en gruppe patologer, som er placenta-eksperter, inkludert Gitta Turowski, utarbeidet de såkalte Amsterdam-kriteriene.2 Gitta har også bidratt til å spre viktigheten av en strukturert rapport i placenta-beskrivelser fra patologen, for at denne skal være til nytte i klinikken.3
Placentamorfologisk undersøkelse må betraktes som ett av flere verktøy fødselslegene kan bruke i sitt kliniske arbeid. Amsterdamkriteriene har hovedfokus på lesjoner av maternell og føtal vaskulær opprinnelse, infeksjon og modningsforstyrrelser, ofte sett ved preeklampsi, veksthemming og abruptio placentae. Hensikten er å gi klinikere et bedre verktøy til å forstå og følge opp svangerskapskomplikasjoner basert på objektive patologiske funn. Placentaeksperter er enige om at det er klinikerne (fødelegene) som er best egnet til å konkludere basert på de samlete undersøkelsene, ved postpartum-samtaler med pasienten. Ikke minst også for å gi anbefaling om oppfølging ved et nytt svangerskap (inkludert forebygging av tidlig preeklampsi med oppstart av lavdose acetylsalicylsyre en eller gang rundt svangerskapsuke 11-14).
To kliniske eksempler på at placentamorfologiske undersøkelser kan være nyttig for legen og pasient:
- Som vakthavende fødelege har du nettopp forløst et barn med vakuum, grunnet truende asfyksi-mistanke på grunn av patologisk CTG. Forløsningen gikk greit, men du synes barnet var overraskende slapt basert på normal CTG tidligere i fødselsforløpet. Ved inspeksjon av placenta er du usikker på en liten kompresjon på maternell flate, og om det kan være noen placentainfarkter. Du sender placentaen til patologen, med opplysninger om problemstilling og svangerskapslengde.
Henvising: Frisk 33 år gammel førstegangsfødende kvinne med spontan fødselsstart uke 37+0. Tilkommet patologisk CTG ved fullåpen cervix. Ukomplisert vakuumforløsning. Apgar 3-5-7 og barnet (2.2 kilo) overflyttes nyfødtavdeling for observasjon. Maternell flate av placenta (som ikke syntes løs ved forløsning av barnet) viser mulig impresjon og mulige infarkter. Tentativ diagnose: Placentadysfunksjon/abruptiotegn og infarkter?
Svaret fra patologen sier: Vurdering: Placenta viste makroskopisk en impresjon på maternell flate, som passer med en tidligere gjennomgått blødning. Mikroskopisk ses tottene i dette arealet degenerert (infarsert). Trofoblastepitelet for øvrig viser økt antall syncytiale knuter og lite antall føtale kar, passende med maternell og føtal sirkulasjonsforstyrrelse. Blødningen kan stå i sammenheng med en overfladisk implantasjon i uterussengen. I tillegg kan den retroplacentære blødningen ha hatt en bidragende effekt på sirkulasjonsforstyrrelsen og dårlig/slapt barn.
Spiralarterier i vedliggende decidua er ikke sett.
Diagnose: Placenta med maternell og føtal vaskulær malperfusjon.
Hva kommuniserer du til foreldrene til barnet? Her vil legeskjønnet ditt og de kliniske funnene rettlede deg om når du tar en samtale med barnets foreldre, og hva som bør diskuteres av placentafunn. Ditt valg om oppfølging avhenger antakelig av fødselsutfallet for det nyfødte barnet, eventuell postpartum preeklampsiutvikling hos mor (her hadde hun ingen preeklampsidiagnose ved forløsning) og selvfølgelig av informasjonsbehovet til barnets foreldre. Her tenker du kanskje at placentafunnene henger godt sammen med barnets fødselsvekt, som var under 2.5-percentilen. Du vet også at placenteringsproblemer øker risikoen for abruptio.
Denne kvinnen rakk kanskje ikke å utvikle preeklampsi eller gestasjonshypertensjon, men kunne ha gjort det, om placenta ikke hadde blitt forløst allerede ved uke 37+0. I et neste svangerskap kan det hende at kvinnen ikke skårer nok poeng til at lavdose acetylsalisylsyre er anbefalt. Fordelen med en mer presis preeklampsi-prediksjonsalgoritme, som for eksempel Fetal Medicine Foundation-algoritmen,4 som allerede er innført i noen land og testet ved St. Olavs hospital i Norge, er at placentafunksjonsfunn også inkluderes. I denne algoritmen vil måling av proteinet PLGF (Placenta Growth Factor), PI av arteria uterina og kvinnens MAP (mean arterial blood pressure) vurderes sammen med obstetrisk og medisinsk historie, samt egenskaper ved kvinnen (BMI etc). Algoritmen gir en samlet risikoskår for tidlig preeklampsi som vil veilede klinikerens eventuelle anbefaling om lavdose aspirinbruk i neste svangerskap. Hadde denne kvinnen vært screenet slik i det aktuelle svangerskapet, kunne det KANSKJE ha medført aspirinbruk, og mulighet for en bedre placentering og mindre placentadysfunksjonsutvikling (medfølgende lavere risiko for abruptio og infarkter). - Sjeldne funn: VUE: Som overlege hadde du ansvaret for et akutt sectio hos en førstegangsfødende i uke 31, der barnet var sterkt tilveksthemmet allerede fra uke 26. Svaret fra patologen overrasker deg, fordi den konkluderer med «villitt av ukjent årsak (VUE: villitis of uknown etiolgy)». Du søker i litteraturen og finner at VUE5 er en sjelden inflammatorisk placentatilstand.6 Hovedkjennetegnet til VUE er infiltrasjon av maternelle immunceller i placentas villøst vev. Slike placentaforandringer tidlig i svangerskapet øker risikoen for alvorlige obstetrisk utfall, inkludert fosterdød. Disse placentaforandringene kan i dag bare identifiseres ved morfologisk undersøkelse av placenta etter forløsning. VUE er assosiert med høy grad av gjentakelse i neste svangerskap, og dermed dårlig obstetrisk utfall.
VUE-diagnosen kan bare settes når en infeksiøs årsak er utelukket. VUE blir vanligere med økende gestasjonsalder og kan da ofte ses ved normale svangerskapsutfall. Men, dersom det påvises alvorlig VUE ved prematur fødsel, slik som i denne sykehistorien, er dette oftest assosiert med risiko for gjentagende alvorlig tilveksthemming og intrauterin fosterdød. Du søker hjelp hos erfarne kollegaer i Norge og har lest at evidensen for å effektivt kunne forebygge dette i neste svangerskap er lav. 6 7 Noen mindre studier har prøvd ut forskjellige kombinasjoner av prednisolon, hydroksyklorokin, tacrolimus, og intravenøs immunoglobulin og adalimumab. Doseringene varierer og resultatene er ikke entydige.
Hvordan informerer du og følger opp pasienten? Du forklarer pasienten at VUE er en sjelden tilstand i morkaken og at årsaken er uklar. En hypotese er at morens immunceller (T-celler) angriper fostercellene i morkaken. Du forteller at det ikke er god evidens for behandling i neste svangerskap, men at noen gravide med veldig alvorlige svangerskapskomplikasjoner (for eksempel fosterdød flere ganger) har blitt med i studier der flere typer immundempende medikamenter er blitt prøvd. Lavdose aspirin, kombinert med lavmolekylært heparin og kortikosteroider har vært prøvd, men også intravenøs immunglobulin (IVIG), hydroksoklorokin og betennelsesdempende legemidler (såkalte biologiske legemidler, som målrettet demper deler av immunsystemet for å redusere betennelse ved autoimmune sykdommer).
Du blir enig med pasienten om å avvente vurdering av oppstart av slike medikamenter, fordi evidensen for dem er begrenset. Det kan jo hende at det er blitt gjort flere kliniske studier som kan rettlede forebygging bedre, neste gang hun er gravid. Du forteller henne at hun sannsynligvis vil tilbys oppstart med acetylsalicylsyre, og at hun også vil tilbys tilvekstvurdering av fosteret med ultralyd.
C) Mikrobiologisk undersøkelse
Veilederen sier: «Vi anbefaler mikrobiologisk undersøkelse av placenta utføres ved manifest/mistenkt infeksjon, premature rier/prematur fødsel med mulig infeksjonsårsak og intrauterin fosterdød».
Et klinisk eksempel: En kvinne kommer inn med premature rier og vannavgang i uke 30. CTG er patologisk og barnet fødes ved akutt keisersnitt, med lav Apgar-skår og behov for neonatal overvåkning. Etter fødselen utvikler moren feber og infeksjonstegn, som gjør at du mistenker chorioamnionitt som årsak til preterm prematur fødsel. Du sender inn prøve av fostervann og placentabiopsi (du følger retningslinjene i Veiledere for prøvetaking og forsendelse, og beskriver PPROM og akutt keisersnitt-forløsning, noe som er viktig for mikrobiologen for å tyde oppvekstfunnene).1
Svaret fra mikrobiologen viser gruppe B-streptokokker og patologens svar er forenelig med chorioamnionitt. Dette styrker diagnosen om infeksjonsutløst prematur fødsel og foreldrene får en bedre forståelse av årsaken til den premature fødselen. Antibiotikavalg hos mor og barn kan også påvirkes av mikrobiologiske funn.
Til slutt
Vi håper disse fiktive, kliniske eksemplene har vært inspirerende og opplysende for deg som kanskje river deg i håret over placentaremisser. Vi håper du, med ny energi, vil beskrive den ferskfødte placentaen, og vurdere indikasjon for å sende den til videre undersøkelser, der dette er nyttig for forståelse av dette svangerskapet, eller eventuell videre behandling og oppfølging i påfølgende svangerskap.
Referanser
1. Staff A HA, Turowski G, Gammelsrud KW, Barlinn R, Ernsting V. Placenta. Veileder i Fødselshjelp 2000 (accessed Oktober 21 2025).
2. Khong TY, Mooney EE, Ariel I, et al. Sampling and Definitions of Placental Lesions: Amsterdam Placental Workshop Group Consensus Statement. Arch Pathol Lab Med 2016; 140(7): 698-713.
3. Turowski G, Tony Parks W, Arbuckle S, Jacobsen AF, Heazell A. The structure and utility of the placental pathology report. APMIS 2018; 126(7): 638-46.
4. Foundation TFM. Risk assessment for preeclampsia. https://fetalmedicine.org/research/assess/preeclampsia/first-trimester (accessed June 9 2020).
5. Derricott H, Jones RL, Greenwood SL, Batra G, Evans MJ, Heazell AE. Characterizing Villitis of Unknown Etiology and Inflammation in Stillbirth. Am J Pathol 2016; 186(4): 952-61.
6. Cornish EF, McDonnell T, Williams DJ. Chronic Inflammatory Placental Disorders Associated With Recurrent Adverse Pregnancy Outcome. Front Immunol 2022; 13: 825075.
7. Mekinian A, Kolanska K, Cheloufi M, et al. Chronic Villitis of unknown etiology (VUE): Obstetrical features, outcome and treatment. J Reprod Immunol 2021; 148: 103438.




